A napi egy adagban alkalmazott Flebaven® (diozmin) 1000 mg hatásossága és biztonságossága krónikus vénás betegségben szenvedő betegeknél
14. 2. 2020
ABSZTRAKT
KULCSSZAVAK: mikronizált diozmin, krónikus vénás betegség, lábfájdalom, hatásosság, biztonságosság
HÁTTÉR. A krónikus vénás betegség gyakori krónikus, nem fertőző betegség, amelynek globális prevalenciája meghaladja a 80 százalékot. Klinikailag az alsó végtagok felületes és/vagy mélyvénáiban lévő megnövekedett vérnyomás által okozott tünetek és jelek összességeként határozható meg. A leggyakoribb tünetek és jelek közé tartozik a lábfájdalom, a nehézláb-érzés és a lábszárak dagadása. A flavonoidok, különösen a mikronizált diozmin, olyan gyógyszerek, amelyek klinikailag bizonyított hatásosságot mutatnak a krónikus vénás betegség kezelésében. A Flebaven® gyógyszerkészítmény klinikai vizsgálatának célja a napi egy adagban alkalmazott Flebaven® 1000 mg hatásosságának és biztonságosságának megerősítése volt krónikus vénás betegségben szenvedő betegeknél. MÓDSZEREK. A klinikai vizsgálatba 389, primer krónikus vénás betegségben és lábfájdalomban szenvedő beteget vontak be. A betegeknek három viziten kellett részt venniük a vizsgálóorvosoknál: a kezelés kezdetén (1. vizit), a kezelés 4. hetében (2. vizit) és a kezelés 12. hetében (3. vizit). A vizsgálóorvosok a tünetek (lábfájdalom, nehézláb-érzés, lábduzzanat intenzitása) numerikus skálán történő felmérésével értékelték a kezelés hatékonyságát. Emellett, az állapot súlyosságát, illetve javulását CGI-S (Klinikai Globális Összbenyomás – Súlyosság Skála; Clinical Global Impression Scale – Severity) és CGI-I (Klinikai Globális Összbenyomás – Javulás Skála; Clinical Global Impression Scale – Improvement) alapján is definiálták. A klinikai vizsgálat kezdetén és végén a betegek az SF-20 kérdőív segítségével értékelték az életminőségüket. A gyógyszer biztonságosságának monitorozása céljából a vizsgálóorvosok mindkét kontrollvizsgálat alkalmával rögzítették a nemkívánatos eseményeket. EREDMÉNYEK. A lábfájdalom ≥ 30%-kal csökkent, illetve a numerikus értékelő skála szerinti pontszám nem haladta meg a 3-as értéket 4 hetes kezelés után a betegek 52%-ánál és 12 hetes kezelés után a betegek 85,4%-ánál. Továbbá a kezelés 12 hete alatt statisztikailag szignifikáns csökkenést figyeltek meg a lábfájdalom intenzitásában, a nehézláb-érzésben és a lábduzzanatban. Az eredmények a betegség súlyosságának statisztikailag szignifikáns csökkenését is kimutatták (a kezdeti 3,326-os értékről 2,350-re csökkent 12 hetes kezelés után; p<0,001). A 4 hetes kezelés utáni átlagos CGI-I pontszám 2,262-ről 1,766-re csökkent 12 hetes kezelés után. A betegek életminősége javult a kezelés végére, a legnagyobb pozitív hatást a fájdalom intenzitásának csökkenésében figyelték meg. A betegek jól tolerálták a Flebaven® kezelést, és 89%-uknál nem jelentkeztek Flebaven® kezeléssel kapcsolatos mellékhatások. KÖVETKEZTETÉSEK. A klinikai vizsgálat eredményei azt mutatták, hogy a napi egy adagban alkalmazott Flebaven® 1000 mg hatásos és a betegek által jól tolerált gyógyszer a krónikus vénás betegség kezelésére.
BEVEZETÉS
A krónikus vénás betegség (CVD) a betegség valamennyi stádiumát magában foglalja a hajszálértágulattól, a varicosus (visszeres) vénákon és az ödémákon át a bőrfekélyekig, míg a krónikus vénás elégtelenség (CVI) a betegség előrehaladott stádiumára utal, amelyet tartós duzzanat és fekélyképződéssel járó bőrelváltozások jellemeznek (1, 2). A CVD klinikailag az alsó végtagok felületes és/vagy mélyvénáiban lévő megnövekedett vérnyomás által okozott tünetek és jelek összességeként határozható meg. A CVD tünetei közé tartozhat a nehézláb-érzés, a lábakban jelentkező tompa fájdalom, viszketés és fáradtság, az éjszakai görcsök és nyugtalan láb szindróma. A CVD-t a következő klinikai tünetek jellemzik: hálózatos vagy varicosus vénák, ödéma és bőrelváltozások, mint a hiperpigmentáció, lipodermatoszklerózis, hiposztatikus dermatitisz és vénás lábszárfekély (1, 2). A CVD progresszív betegség. Amennyiben nem kezelik időben, a betegség súlyosabb formájává fejlődhet. (3)
A CVD osztályozására több rendszert is kidolgoztak. A részletesebb CEAP-skála a betegség klinikai (C), etiológiai (E), anatómiai (A) és patofiziológiai (P) szempontjait veszi figyelembe (1, 4). A klinikai osztályozás a CVD klinikai tüneteit veszi figyelembe, és hét csoportot foglal magában (1. táblázat). A C mellett alsó indexben feltüntetett betű a tünetek jelenlétét (s) vagy távollétét (a) jelzi. Az etiológia a veleszületett (Ec), primer (Ep) vagy szekunder (Es) kategóriákba sorolható. Az anatómiai osztályozás a felületes, mély vagy perforáns vénák érintettsége alapján történik. A CVD alapját képező patofiziológia a refluxhoz (r), vagy az elzáródáshoz (o), vagy mindkettőhöz (r + o) kapcsolódik.
1. táblázat: CEAP klinikai osztályozás, amely magában foglalja a betegség klinikai, etiológiai, anatómiai és patofiziológiai szempontjait. CEAP – klinikai, etiológiai, anatómiai, patofiziológiai (a CVD átfogó osztályozási rendszere)

A CVD gyakori krónikus, nem fertőző betegség, amelynek globális prevalenciája meghaladja a 80%-ot: a betegek több mint 60%-ánál CEAP C1–C6 fokozatú CVB-t diagnosztizálnak, és a betegek kb. 20%-ánál CEAP C0 fokozatú primer CVB-t diagnosztizálnak (5). A CVB kezelésében klinikailag bizonyított hatásosságú gyógyszerkészítmények a flavonoidok, különösen a mikronizált diozmin (6). A Flebaven® mikronizált diozmin hatóanyagot tartalmaz (7). A < 10 µm átmérőjű részecskéket eredményező mikronizálási folyamat javítja a diozmin gyomor-bélrendszeri felszívódását és következésképpen a készítmény biohasznosulását és klinikai hatásosságát (8, 9). A mikronizált diozmin orális biohasznosulása kb. 60% (7).
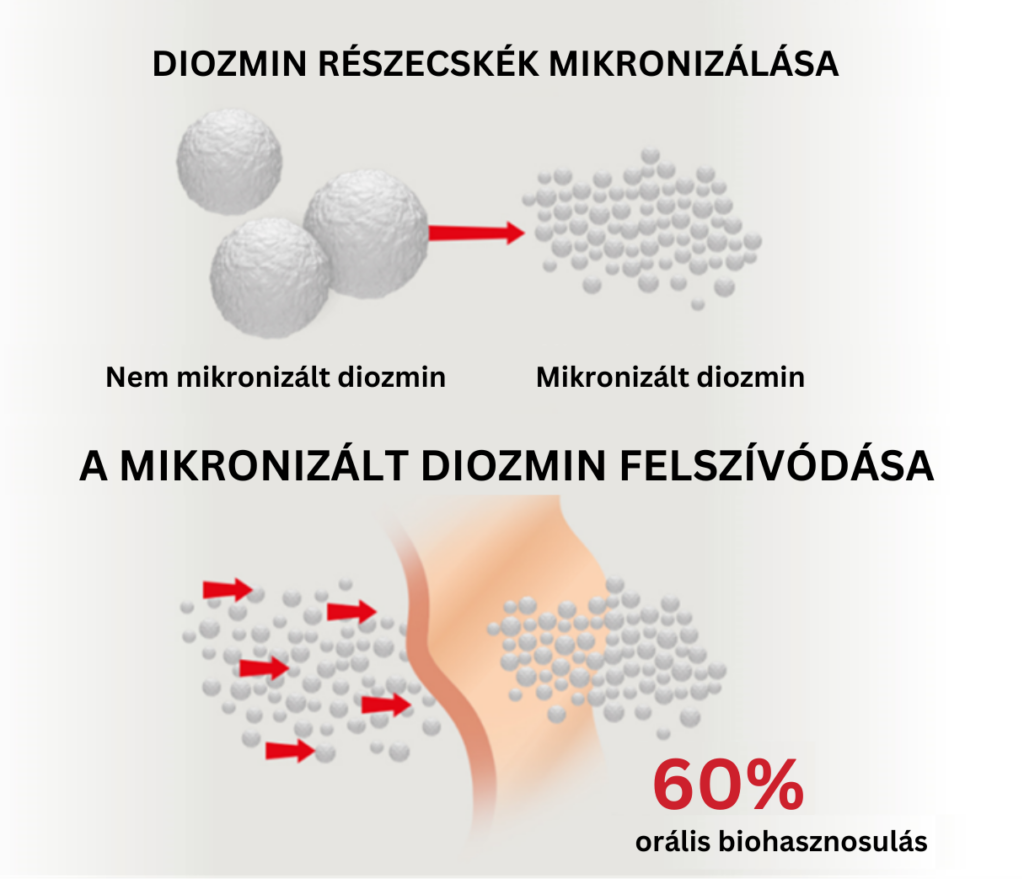
1. ábra: A mikronizált diozmin gyomor-bélrendszeri felszívódásának diagramja
A mikronizált diozmin felnőtteknél a krónikus vénás betegség jeleinek és tüneteinek, mint például lábfájdalom, nehézláb-érzés, fáradt vagy nyugtalan lábak, görcsök, ödéma és trophicus zavarok kezelésére, valamint az akut aranyeres betegséghez kapcsolódó tünetek kezelésére javallott (7).
A mikronizált diozminról kimutatták, hogy növeli a vénás tónust, és csökkenti a vénás kapacitást, a disztenzibilitást és a pangást. A higanyos nyúlásmérővel végzett vénás occlusio plethysmographia a vénás ürítési idő csökkenését mutatta. A mikronizált diozmin a vénás mikrokeringésre is hatással van, mivel csökkenti a kapillárisok permeabilitását és növeli a kapilláris ellenállást. Gyulladáscsökkentő tulajdonságokat mutat, mivel befolyásolja a prosztaglandinok szintézisét. Mindezek eredményeként elősegíti a vénás hipertónia csökkentését a vénás betegségben szenvedő betegeknél (7).
A mikronizált diozmin hatásosságát különböző klinikai vizsgálatokban tesztelték. Ziaja és munkatársai kimutatták, hogy a gyógyszerkészítmény hatásos a CVD-ben szenvedő betegeknél. Nyílt elrendezésű, nem összehasonlító klinikai vizsgálatukba 6569 beteget vontak be, akiknek monitorozását 330 háziorvosi rendelőben végezték. A vizsgálat kimutatta, hogy a mikronizált diozmin hatásos a CVD tüneteinek csökkentésében, mivel a betegek a lábfájdalom, a nehézláb-érzés statisztikailag szignifikáns csökkenéséről, a lábdagadás, a görcsök és a nyugtalan láb jelentette panaszok mérséklődéséről számoltak be. Emellett a mikronizált diozmin hatásosan csökkentette a boka és a vádli körfogatát (10).
A klinikai vizsgálat célja a naponta egyszer alkalmazott Flebaven® 1000 mg hatásosságának és biztonságosságának megerősítése volt CVD-ben szenvedő betegeknél.
MÓDSZEREK:
A prospektív, nyílt elrendezésű, multicentrikus, intervenciós klinikai vizsgálatot 2018 júniusa és 2019 júliusa között végezték Szlovéniában. A vizsgálatba olyan 20 és 70 év közötti, primer CVD-vel diagnosztizált betegeket vontak be, akiknek az NRS-skála szerinti átlagos lábfájdalma 4-es vagy annál erősebb volt (közepes vagy súlyos fájdalom), és akiknek a CEAP besorolása (a súlyosabban érintett lábra vonatkozóan) C0 és C4 között volt. A kizárási kritériumok a következők voltak: a hatóanyaggal vagy bármely segédanyaggal szembeni túlérzékenység; C5 és C6 közötti CEAP besorolás (a súlyosabban érintett láb esetében); egyidejűleg alkalmazott nem farmakológiai kezelés (szkleroterápia, visszérműtét, angioplasztika, endovaszkuláris eszköz); és a vizsgálatba való bevonás előtt kevesebb, mint 3 hónappal befejezett nem farmakológiai kezelés. További kizárási kritériumok voltak a következők: alsó végtagokat érintő nyiroködéma; veseelégtelenség vagy dekompenzált szívelégtelenség; májkárosodás; enterectomia a kórtörténetben; nem megfelelő étrend; felszívódási zavar; aktív vénatrombózis; és jelentős krónikus mélyvénás elzáródás, amely vénás sántításhoz és jelentős kompressziós kezeléshez vezethet, súlyos gyulladásos betegség; vagy az alsó végtagok fájdalmának egyéb oka. A klinikai vizsgálatból kizárták az egyidejűleg gyulladáscsökkentő kezelésben részesülő betegeket (kivéve azokat, akik < 350 mg/nap acetilszalicilsav adagot kaptak trombocita-aggregáció gátló kezelésként); a szisztémás kortikoszteroidokat; az immunszuppresszánsokat és a venoaktív gyógyszerkészítményeket használó betegeket; a bevonást megelőző hónapban bevezetett vagy módosított egyidejű ópiát kezelésben részesülő betegeket; valamint a terhes és a szoptató nőket, illetve azokat a nőket, akik nemrégen (a bevonást megelőző legfeljebb 6 hónapban) szültek.
Azok a betegek, akik aláírták a klinikai vizsgálatban való részvételre vonatkozó beleegyező nyilatkozatot, és megfeleltek a bevonási kritériumoknak, 12 hetes Flebaven® kezelésben vettek részt. A betegek naponta 1 Flebaven® 1000 mg tablettát vettek be a nap bármely szakában, de mindig ugyanabban az időben (± 3 óra) és étkezés során.
A betegeknek három viziten kellett részt venniük a vizsgálóorvosoknál – a kezelés kezdetén (1. vizit, kiindulás) és a kezelés alatt (két kontroll vizit): a kezelés 4. hetében (2. vizit) és a kezelés 12. hetében (3. vizit). Az 1. vizit során az orvosok az általános kórtörténet áttekintésével, valamint a lábfájdalom súlyosságának az NRS-skála (2. táblázat) és a CEAP besorolás (1. táblázat) szerinti értékelésével ellenőrizték, hogy a betegek megfelelnek-e a beválasztási és a kizárási kritériumoknak.
2. táblázat: A CVD egyik tünetét – a lábfájdalmat – értékelő numerikus skála.
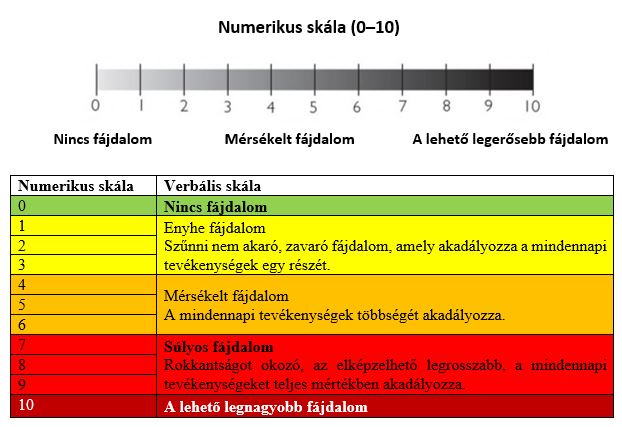
A kontrollvizsgálatok során a vizsgálóorvosok a kezelés hatásosságát három skálán értékelték: a CVD tüneteit (lábfájdalom, nehézláb-érzés, lábduzzanat súlyossága) az NRS-skála segítségével; a betegség súlyosságát a CGI-S skála segítségével (1 = nem beteg, 7 = nagyon beteg); és a betegség javulását a CGI-I skála segítségével (1 = nagyon sokat javult, 7 = nagyon sokat romlott) értékelték.
A klinikai vizsgálat kezdetén és végén a betegek az SF-20 kérdőív kitöltésével értékelték az életminőségüket a Rand Corporation által a Medical Outcomes Study (MOS) számára kifejlesztett, az egészséggel kapcsolatos életminőséget vizsgáló, 20 tételes rövid kérdőív (20-Item Short Form Survey Instrument, SF-20ct).
A biztonságossági profil értékelése céljából a klinikai vizsgálat teljes időtartama alatt monitorozták a mellékhatásokat. A vizitek során a vizsgálati készítmény biztonságosságát a beteginterjúk részeként nyert adatok alapján is értékelték. Az értékelt és elemzett megfigyelt biztonságossági események a mellékhatások általános incidenciája és a gyógyszerkészítmény mellékhatásainak gyakorisága volt típusuk szerint, illetve azon betegek százalékos aránya szerint bontva, akik nem szakították meg a kezelést a mellékhatások miatt. A nemkívánatos eseményeket a gyógyszerrel való kapcsolat, az intenzitás, a súlyosság, a megjelenésig eltelt idő, a gyakoriság, a kezelés szükségessége és a mellékhatás várhatóságának mértéke szerint osztályozták.
A klinikai vizsgálat elsődleges végpontja a ≥ 30%-kal alacsonyabb lábfájdalom intenzitást észlelő betegek hányadának meghatározása volt (NRS-pontszám, 2. táblázat), vagy azon betegek százalékos arányának meghatározása, akiknél az NRS-pontszám ≤ 3 volt (időpontok: kiindulás, 4. hét és 12. hét).
A klinikai vizsgálat során monitorozott másodlagos végpontok közé tartozott a jelentett lábfájdalom intenzitásának, a nehézláb-érzésnek és a lábduzzanat súlyosságának különbsége (az NRS-skála segítségével értékelve) a klinikai vizsgálat kezdete és vége között (időpontok: kiindulás, 4. hét és 12. hét); az életminőség különbsége (az SF-20 kérdőív segítségével értékelve) a klinikai vizsgálat kezdete és vége között; a betegség súlyosságának különbsége (a CGI-S skálával értékelve) a klinikai vizsgálat kezdete és vége között (időpontok: kiindulás, 4. hét és 12. hét); és a betegség javulásának különbsége (a CGI-I skálával értékelve) a klinikai vizsgálat kezdete és vége között (időszakok: kiindulás, 4. hét és 12. hét). Egy 25 betegből álló, látható CVD-tüneteket (visszeresség, ödéma) mutató alcsoportban a vizsgálóorvosok a klinikai vizsgálat kezdetén és a kezelés 12. hete után fényképfelvételek formájában rögzítették a bizonyítékokat.
EREDMÉNYEK
A klinikai vizsgálatban 389 beteg vett részt; 72 férfi (18,5%) és 317 nő (81,5%). A vizsgálatba bevont betegek átlagos életkora 56,3 év volt (1. kvartilis: 50; 3. kvartilis: 65). A CEAP besorolás alapján a betegek többsége C2 (36%) és C3 (30,8%) fokozatú CVD-vel rendelkezett.
A klinikai vizsgálati tervvel összhangban a CEAP C0-C4 fokozatú betegeket vonták be. A betegek 8,2%-a részesült korábbi CVD-kezelésben.
Hatásosság
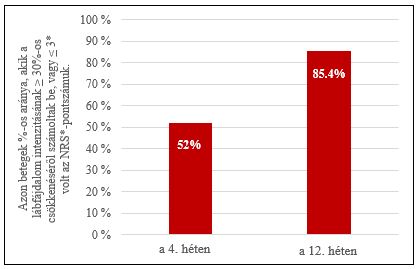
Az elsődleges végpontot teljesítő betegek aránya (azon betegek aránya, akik a kiindulási értékhez képest ≥ 30%-kal alacsonyabb lábfájdalom intenzitásról számoltak be, vagy ≤ 3 volt az NRS-pontszámuk) 4 hetes kezelés után 52% volt, 12 hetes kezelés után pedig 85,4% (2. ábra).
2. ábra: Az elsődleges végpontot elérő betegek aránya a 4 hetes és a 12 hetes kezelés után a kiindulási értékhez képest (NRS).
Statisztikailag szignifikáns csökkenést mutattak ki 4 hetes és 12 hetes kezelés után a lábfájdalom súlyossága, a nehézláb-érzés és a lábduzzanat intenzitása tekintetében (az NRS-skála segítségével értékelve) (p<0,001), amint az a 3. ábrán látható.
3. ábra: A CVD-tünetek (lábfájdalom, nehézláb-érzés, lábduzzanat) alacsonyabb intenzitása (NRS)
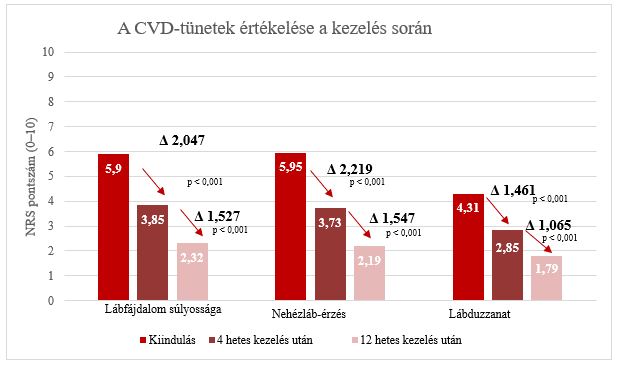
A lábfájdalom intenzitásának kezdeti értéke 5,897 volt. 4 hetes kezelés után 3,850, 12 hetes kezelés után pedig 2,323 volt a lábfájás intenzitása. 4 hetes kezelés után 167 beteg (42,9%), 12 hetes kezelés után pedig 298 beteg (76,4%) nem jelentett fájdalmat vagy csak enyhe fájdalmat jelentett (0–3 NRS-pontszám) (4. ábra).
4. ábra: Fájdalomintenzitás pontszámot adó betegek száma az egyes viziteken. NRS – Numerikus skála
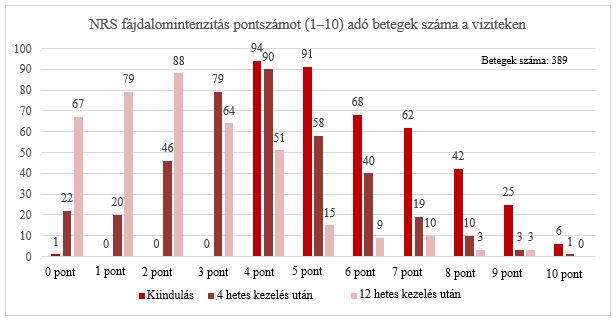
A nehézláb-érzést 5,956 pontra értékelték az 1. viziten. 4 hetes kezelés után 3,737, 12 hetes kezelés után pedig 2,190 volt a nehézláb-érzés intenzitása. Az NRS-skála (0 10) alapján kapott pontszámok eloszlása azt mutatja, hogy 4. és 12. hetes kezelés után – a kiindulási értékhez képest – megnőtt a 0 és 3 közötti pontszámok aránya (ezek a pontszámok enyhe nehézláb-érzést definiálnak), a 4-es és annál magasabb pontszámok aránya pedig csökkent, ami azt jelenti, hogy csökkent a közepes vagy súlyos nehézláb-érzést tapasztaló betegek száma. 4 hetes kezelés után 185 beteg (47,5%), 12 hetes kezelés után pedig 310 beteg (79,6%) számolt be arról, hogy nem volt nehézláb-érzése vagy csak enyhe nehézláb-érzése volt (1–3 NRS pontszámok).
5. ábra: NRS nehézláb-érzés pontszámot (1–10) adó betegek száma a viziteken. NRS – Numerikus skála
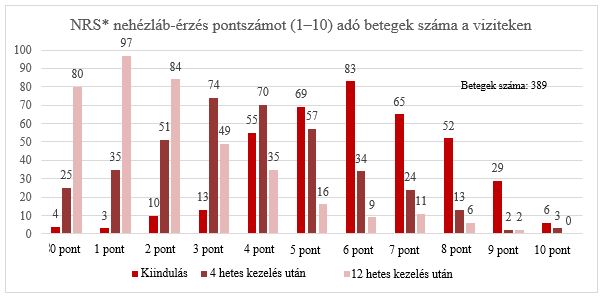
| Betegek száma: 389 |
A lábduzzanat súlyosságát 4,311 pontra értékelték az 1. viziten. 4 hetes kezelés után 2,850, 12 hetes kezelés után pedig 1,785 volt a lábduzzanat intenzitása. 4 hetes kezelés után 260 beteg (67%), 12 hetes kezelés után pedig 326 beteg (84%) nem jelentett ödémát vagy csak enyhe ödémát jelentett (1–3 NRS-pontszám) (6. ábra).
6. ábra: Lábduzzanat intenzitás pontszámot (1–10) adó betegek száma a viziteken. NRS – Numerikus skála
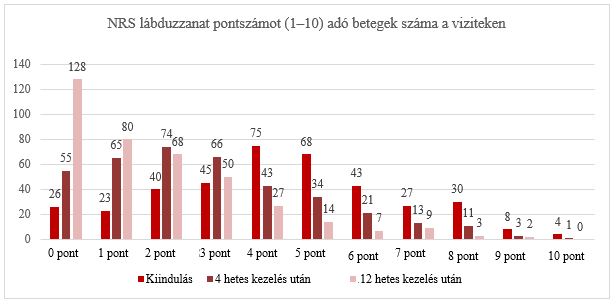
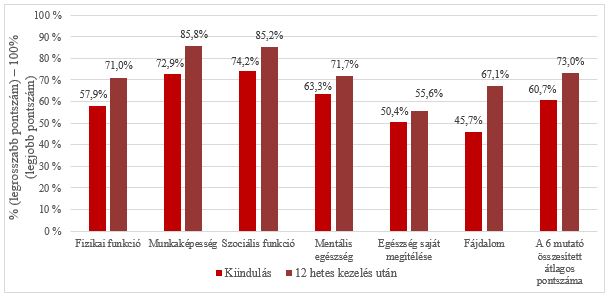
A klinikai vizsgálat kezdetén és végén a betegek az SF-20 kérdőív kitöltésével értékelték az életminőségüket. Az életminőséggel kapcsolatos valamennyi mutatóban (fizikai funkció, munkaképesség, szociális funkció, mentális egészség, egészség saját megítélése, fájdalom) statisztikailag szignifikáns javulást mutattak ki 12 hetes kezelés után a vizsgálat kezdetén kapott alapszint értékekhez képest (p<0,001). A hat (6) mutatót a 0–100%-os intervallumban pontozták (100% = legmagasabb pontszám, 0% = legalacsonyabb pontszám) (7. ábra).
A Flebaven® kezelés a fájdalomintenzitás csökkentésére gyakorolta a legnagyobb pozitív hatást. A pontszám 21,4 százalékponttal, 45,7%-ról 67,1%-ra nőtt. A magasabb pontszám azt jelenti, hogy a betegek kevesebb fájdalmat tapasztaltak, vagy a tapasztalt fájdalom kevésbé befolyásolta az életminőségüket. Összességében 12 hetes kezelés után az életminőség 11,8 százalékponttal, 60,7%-ról 73%-ra javult (a kiinduláshoz képest).
7. ábra: Életminőségi mutatók értékelése a kiinduláskor és 12 hetes kezelés után
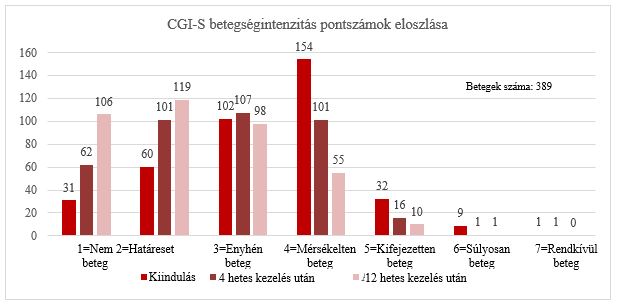
A vizsgálóorvosok a betegség súlyosságának különbségét is monitorozták (a CGI-S skála segítségével értékelve) a klinikai vizsgálat teljes időtartama alatt. A betegség súlyossága a kiindulási értékhez képest statisztikailag szignifikánsan csökkent 4 hetes és 12 hetes kezelés után is (p<0,001). A betegség súlyosságának pontszáma 4 hetes kezelés után a kiindulási értékről (3,326) 2,784-re, 12 hetes kezelés után pedig 2,350-re csökkent. A betegség súlyosságának a CGI-S skála alapján értékelt változása 12 hetes kezelés után a kiindulási pontszámmal összehasonlítva a „Nem beteg” kategóriában volt a legnagyobb. A kiindulási érték ebben a kategóriában 8% volt (31 beteg). 12 hetes kezelés után a pontszám 27,1%-ra nőtt (106 beteg). A különbség statisztikailag szignifikáns (p<0,001)
8. ábra: A súlyossági értékelések eloszlása. CGI-S – Klinikai összbenyomás skála – Súlyosság
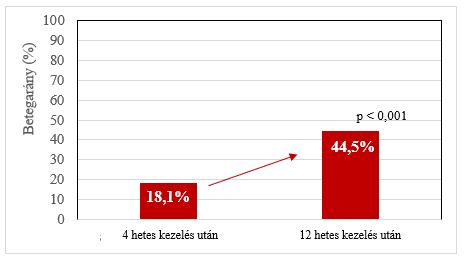
A vizsgálóorvosok 4 hetes kezelés és 12 hetes kezelés után is értékelték a betegség javulásának különbségét (a Klinikai összbenyomás skála – Súlyosság (CGI-S) segítségével). 4 hetes kezelés és 12 hetes kezelés után is statisztikailag szignifikáns csökkenést mutattak ki az átlagos CGI-S pontszámban (p<0,001). Az alacsonyabb átlagos pontszám a betegség javulását jelzi. A 4 hetes kezelés utáni átlagos CGI-I pontszám 2,262-ről 1,766-ra csökkent 12 hetes kezelés után. A betegek a 4 hetes kezelés utáni és a 12 hetes kezelés utáni állapotában kimutatott jelentős különbség a „Nagyon sokat javult” kategóriában a legnagyobb, ebben az esetben 18,1%-ról 44,5%-ra emelkedett (9. ábra). A különbség statisztikailag szignifikáns (p<0,001).
9. ábra: A kezelés során a „Nagyon sokat javult” választ adó betegek aránya
Biztonságosság
A Flebaven® biztonságosságát mind a 389 betegnél értékelték. A betegek jól tolerálták a Flebaven® kezelést, és 346 beteg (a betegek 89%-a) nem jelentett a vizsgálati készítménnyel kapcsolatos mellékhatásokat (ADR). Mellékhatásokat 44 betegnél (11,3%) rögzítettek; egy (1) betegnél fordult elő a vizsgálati készítménnyel nem összefüggő mellékhatás; 43 betegnél (11%) 71 mellékhatást rögzítettek. 4 hetes kezelés után, a 2. vizit során 54 mellékhatást rögzítettek. A jelentett mellékhatások túlnyomórészt enyhék voltak (61,1%), és a 12 hetes kezelés utáni 3. vizit idejére megoldódtak. 12 hetes kezelés után csak 23 mellékhatást rögzítettek. A leggyakrabban jelentett mellékhatások a gyomor-bélrendszeri problémák voltak. A ritka mellékhatások közé tartoztak a bőrbetegségek és a neurológiai rendellenességek (fejfájás, álmatlanság, nyugtalan lábak), valamint a gyakori tünetek (rossz közérzet).
DISZKUSSZIÓ
A krónikus vénás betegség gyakori, nem fertőző betegség, amelynek legáltalánosabb tünetei és jelei közé tartozik a lábfájdalom, a nehézláb-érzés és a lábduzzanat. Ez a klinikai vizsgálat kimutatta, hogy a naponta egyszer alkalmazott Flebaven® 1000 mg hatásos gyógyszer a krónikus vénás betegség kezelésére, mivel 4 hetes és 12 hetes kezelés után a betegség tüneteinek és jeleinek (lábfájdalom, nehézláb-érzés és lábduzzanat) statisztikailag szignifikáns regresszióját rögzítették. A lábfájdalom-intenzitás és az oedema csökkenésére gyakorolt hatása szignifikánsan jobb volt 12 hetes kezelés után, mint 4 hetes kezelés után. Ezért indokolt a kezelés meghosszabbítása, különösen a markánsabb tüneteket és jeleket mutató betegek esetében. A kezelés végén a betegek az életminőségük jelentős javulásáról számoltak be, de a legnagyobb pozitív hatást a fájdalomintenzitás csökkenésében figyelték meg. A vizsgálóorvosok megerősítették, hogy 4 hetes és 12 hetes kezelés után statisztikailag szignifikáns javulás következett be a kiindulási értékhez képest.
A betegek jól tolerálták a kezelést, mivel 89%-uk nem jelentett a Flebaven® kezeléssel kapcsolatos mellékhatást. Más vizsgálatokban is hasonló volt a mellékhatások gyakorisága, a betegek leggyakrabban gyomor-bélrendszeri és neurológiai rendellenességekről (fejfájás, szédülés, rossz közérzet, álmatlanság stb.) számoltak be (12).
A mikronizált diozminnal végzett kezelés értékelésének eredményei összhangban vannak más meglévő tanulmányok megállapításaival, amelyek szerint ez a hatóanyag pozitív hatással van a krónikus vénás betegségek tüneteire és jeleire. A vénákat erősítő szerek hatásosságának legutóbbi, 2016-ban befejezett Cochrane metaanalízise azt mutatta, hogy kedvezően hatnak az oedema, a görcsök, a nyugtalan lábak és a paraesthesia regressziójára (11). Az alsó végtagok krónikus vénás panaszainak kezelésére vonatkozó legújabb ajánlásokat 2018-ban tették közzé (3). Ezek hangsúlyozzák a tüneteket mutató betegek venoaktív gyógyszerkészítményekkel való kezelésének fontosságát, ezek önálló kezelésként vagy más terápiákkal, különösen kompressziós terápiával, illetve a krónikus vénás betegség előrehaladottabb stádiumaiban invazív terápiás módszerekkel kombinálva írhatók fel.
KÖVETKEZTETÉS
Ez a klinikai vizsgálat betekintést nyújt egy rendkívül elterjedt betegség, a krónikus vénás betegség Flebaven® kezelésének hatásosságába. Ez az első ilyen klinikai vizsgálat, amelyet Szlovéniában végeztek. A krónikus vénás betegségben szenvedő betegeknél bizonyította a naponta egyszer alkalmazott Flebaven® 1000 mg hatásosságát és biztonságosságát.
Szerzők
- Barbara Krevel, MD, Department of vascular diseases, University Medical Centre Ljubljana, Zaloška 7, 1000 Ljubljana; barbara.krevel@kclj.si
- Breda Barbič-Žagar, MD, Krka, d. d., Novo mesto, Dunajska cesta 65, 1000 Ljubljana
- Nataša Uranič, MPharm, Krka, d. d., Novo mesto, Dunajska cesta 65, 1000 Ljubljana
Irodalom:
- Kecelj Leskovec N, Kozak M, Slana A, et al. Priporočila za odkrivanje in zdravljenje kronične venske bolezni. Zdrav vestn. 2017; 86: 345–61.
- Ramelet AA, Perrin M, Kern P, Bounameaux H. Phlebology. 5th ed. Paris: Elsevier; 2008.
- Nicolaides A, Kakkos S, Baekgaard N, et al. Management of chronic venous disorders of the lower limbs. Guidelines According to Scientific Evidence. Part I. Int Angiol. 2018: 37(3): 181-254.
- Porter JM, Moneta G and International Consensus Comittee on Chronic Venous Disease. Re-porting standards in venous disease. J Vasc Surg. 1995; 21(4): 635–45.
- Rabe E, Guex JJ, Puskas A, et al. Epidemiology of chronic venous disorders in geographically diverse populations: results from the Vein Consult Program. Int Angiol 2012; 31: 105–15.
- Šikovec A, Planinšek-Ručigaj T, Košiček M et al. Smernice za odkrivanje in zdravljenje kroničnega venskega popuščanja. Zdrav vestn. 2005; 74: 193–202.
- Povzetek glavnih značilnosti zdravila Flebaven®, KRKA, tovarna zdravil, d. d., Novo mesto, Šmarješka cesta 6, 8501 Novo mesto, Slovenija. Dosegljivo na:
- https://www.krka.biz/sl/zdravila-in-izdelki/izdelki-brez-recepta/flebaven-1000-mg-filmsko-oblozene-tablete/12814/
- Kumar S, Singh P. Various techniques for solubility enhancement: An overview. The Pharma Innovation Journal 2016; 5(1): 23-8.
- Chaumeil JC. Micronization: A method of improving the bioavailability of poorly soluble drugs. Methods Find Exp Clin Pharmacol.1998; 20 (3): 211-5.
- Ziaja D et al. Effectiveness of using micronised diosmin in the treatment of chronic venous insufficiency in the Polish population. Chirurgia Polska 2012, 14, 1–2,14–23.
- Martinez-Zapata MJ, Vernooij RW, Uriona Tuma SM,et al. Phlebotonics for venous insufficiency. Cochrane Database Syst Rev. 2016 Apr 6;4:CD003229.
- Meyer O. Safety of use of Daflon 500 mg confirmed by acquired experience and new research. Phlebology 1992; 7 Suppl. 2: 64–8.